Kontaktkorrosion / Elektrokorrosion: Ursachen und Hintergründe
Kontaktkorrosion
Korrosion kommt aus dem Lateinischen und heisst zerfressen, zernagen. Kontaktkorrosion wird auch Elektrochemische Korrosion oder Elektrokorrosion genannt. Sie tritt auf wenn zwei unterschiedliche Metalle direkten leitenden Kontakt haben und von einem Elektrolyt wie beispielsweise Wasser umgeben werden. Diese Kombination wird auch ein galvanisches Element genannt und entspricht einer Batterie.
Und genau wie in der Batterie kommt es bei der Kombination von verschiedenen Metallen zu einem Stromfluss über das Metall und einer Ionen-Wanderung durch die Flüssigkeit, den Elektrolyt. Ionen sind winzige Metallteile und Ionenwanderung heisst, das sich Metallteilchen von dem unedleren Metall ablösen und dieses somit zerstört wird. Im Extremfall löst sich das unedlere Metall auf. Das Ablösen der Metallteilchen ist die Korrosion (oft auch Lochfrass).
In der Praxis geschieht dieser Vorgang bei der Verbindung von Rohrleitungen aus unterschiedlichen Metallen. Der Elektrolyt ist das Wasser im Rohr. Es genügt auch feuchte Luft oder eine feuchte Verschmutzung. Die Abwanderung von Ionen aus dem unedleren Rohrleitungsmaterial ist die Korrosion, die wir teilweise als Lochfrass erkennen.
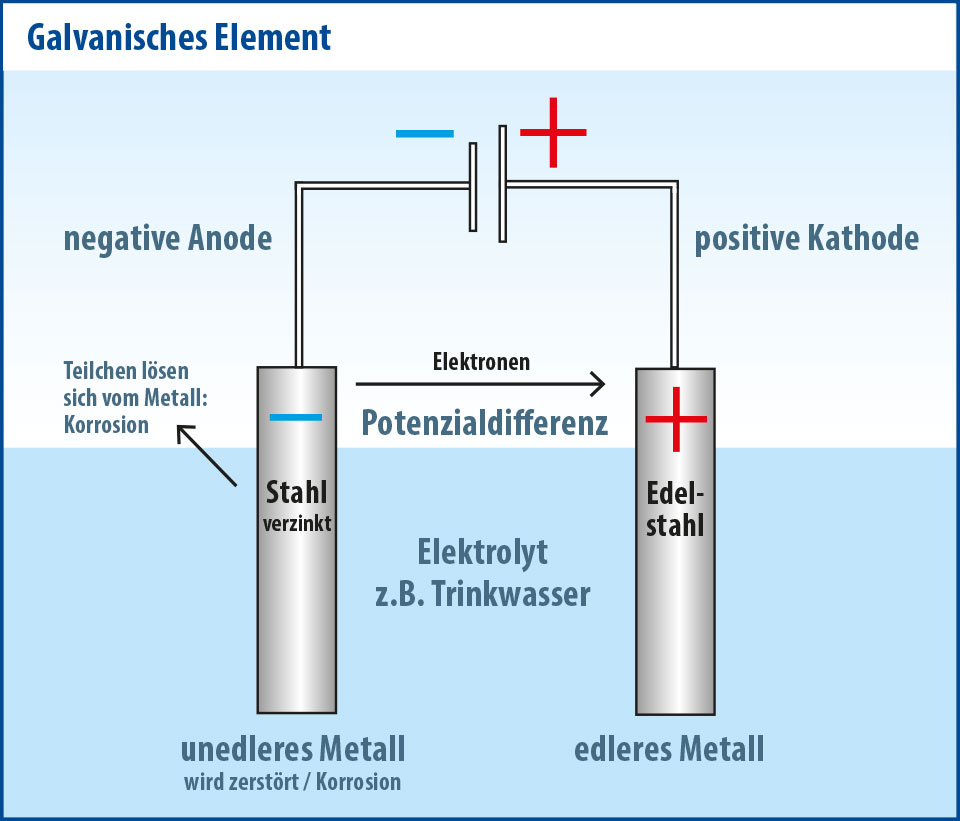

Elektrochemischer Hintergrund bei Kontaktkorrosion
Das unedlere Metall ist in der elektrolytischen Spannungsreihe (siehe Tabelle Spannungsreihe ) negativer und wird zur Anode. Es gibt positiv geladene Metallteilchen in den Elektrolyten ab (Korrosion) und negative Elektronen fliessen über das Metall ab (Stromfluss).
Die negativen Elektronen reagieren an der Kathode mit dem Elektrolyten, in unserem Fall mit dem Wasser. Es entsteht ein Hydoxid (OH-).
Der Chemiker spricht davon das die Anode oxidiert und die Kathode reduziert wird. Das ganze System bezeichnet man auch als Korrosionszelle. Je weiter die beiden Metalle in der elektrolytischen Spannungsreihe von einander entfernt sind (siehe Tabelle Spannungsreihe), um so schneller und „aggressiver“ verläuft die Korrosion.
Abhilfe und Korrosionsschutz
Einfach durch den Einsatz eines KYBURZ® Isolierstückes beim Verbinden von Rohrleitungen aus unterschiedlichen Materialien. Der Stromfluss wird gestoppt
und somit auch das Ablösen der Metallteilchen,
die Korrosion. Die Lebensdauer von Anlagen und
Installationen können somit um ein Vielfaches verlängert werden.
Die KYBURZ® Produkte bieten Langzeit-Korrosionsschutz für Ihre Gebäudeinstallationen, Industrieanlagen und erdverlegten Rohrleitungen.

| Elektrolytische Spannungsreihe – Normalpotentiale gegen Wasserstoff bei 25°C und 101300 Pa | |||||
|---|---|---|---|---|---|
| Spannung (V) | Spannung (V) | ||||
| Gold (Au) | + 1,69 | Molybdän (Mo) | – 0,20 | ||
| Platin (Pt) | + 1,20 | Nickel (Ni) | – 0,25 | ||
| Quecksilber (Hg) | + 0,85 | Edelstahl aktiv | – 0,32 | ||
| Titan (Ti) | + 0,80 | Eisen (Fe) | – 0,41 | ||
| Silber (Ag) | + 0,80 | Gusseisen | – 0,42 | ||
| Kupfer (Cu) | + 0,35 | Stahl verzinkt | – 0,60 | ||
| Edelstahl passiv | + 0,40 | Zink (Zn) | – 0,76 | ||
| Wasserstoff (H2) | + 0,00 | Chrom (Cr) | – 0,91 | ||
| Blei (Pb) | – 0,13 | Aluminium (Al) | – 1,66 | ||
| Zinn (Sn) | – 0,14 | ||||